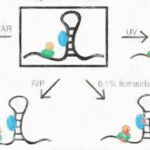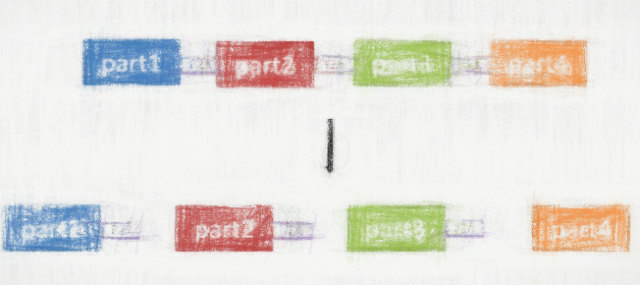
IRESや2Aペプチドを使えば、1つのmRNAから複数のタンパクを発現させることができます。
この記事ではIRESを簡単に紹介してから、2Aペプチドの原理やメリットについてまとめます。
1本のmRNAから複数のタンパクをつくる
バクテリアでは、1つのmRNAから複数の遺伝子が翻訳されていることはさまざまな教科書で、例えばオペロンの説明などで紹介されています。
一方、哺乳類では原則として1つのmRNAからは1つの遺伝子のみが翻訳されています。
しかしながら、遺伝子工学の技術を利用して、1つのmRNAから複数のタンパクを翻訳させることもできます。
この目的のために広く利用されているのが、IRESと2Aペプチドです。
IRES
IRES (internal ribosome entry site) は、ポリオウイルス(PV)と脳脊髄炎ウイルス(EMCV)の RNA ゲノムから1988 年に発見されました。
mRNAの5'末端にはキャップがついていますが、IRES配列はキャップに依存せずに翻訳を行うことができます。
この発見以降、1つのmRNAから2つの遺伝子を発現させるために、IRES配列を2つの遺伝子間に挿入することが一般的になりました。1つ目の遺伝子のstopコドンを除き、IRESを入れ、2つ目の遺伝子のスタートコドンを除くことでポリシストロニックな翻訳が可能です。
この場合、最初の遺伝子は通常の5'キャップ依存的に翻訳され、2番目の遺伝子はIRESで翻訳開始されます。
これまで多数のウイルスからIRESが同定されていて、それらの配列は少しずつ異なっています。例えばEMCVのIRESはこのような配列になっています。
IRESの弱点としては、2つ目の遺伝子の発現量が1つ目の遺伝子に比べて大きく落ち気味 (1/10程度) であり、またIRESが後述の2Aペプチドに比べて長いということです。
2Aペプチド
2Aペプチドは、18-22アミノ酸の長さのウイルス由来のペプチドで、下のwikipediaの図のように2Aペプチドの前後にある2つの遺伝子を1本のmRNAからつくることができます。
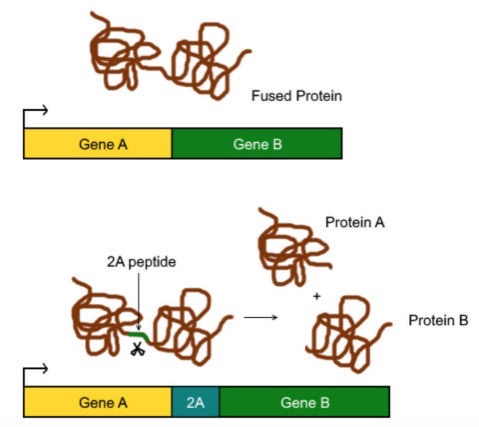
2Aという名前は、ウイルスゲノムの特定の領域の名前に由来します。
さまざまなウイルス由来の2Aがあり、その由来となったウイルスにちなんで命名されています。
最初に発見された2AはF2A(foot-and-mouth disease, 口蹄疫ウイルス)(原著論文は1991年に発表)であり、その後、E2A(equine rhinitis A virus, 馬鼻炎Aウイルス)、P2A(porcine teschovirus-1 2A, 豚テスコウイルス-1 2A)、T2A(thosea asigna virus 2A)が同定されました。最初の3つはピコルナウイルス科ですが、最後のウイルスは昆虫に感染するウイルスです。
それぞれの配列を見てみましょう。
(GSG) EGRGSLLTCGDVEENPGP
P2A
(GSG) ATNFSLLKQAGDVEENPGP
E2A
(GSG) QCTNYALLKLAGDVESNPGP
F2A
(GSG) VKQTLNFDLLKLAGDVESNPGP
いずれの2AもC末にNPGPの配列があり、プロリン(P)とグリシン(G)の間のペプチド結合の間が開裂します。その結果として、2Aペプチドの上流のタンパクのC末には2AのC末のプロリン以外の配列がつき、2Aペプチドの下流のタンパクのN末には2Aペプチド由来のプロリンが1つつきます。
また、先頭のGSGは()で囲んでいますが、この配列はなくても2Aペプチドとして機能するものの、GSGをつけることでその切断効率が上昇することが知られています。特に理由がなければ、GSGをつけた配列を使う方が望ましいと思います。
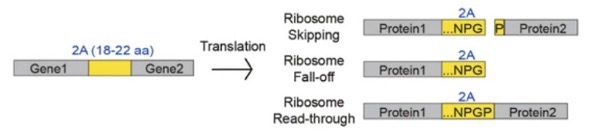
ribosome skippingによって1つのmRNAから2つのタンパクができますが、下流のタンパクが作られない場合、1つの融合タンパクもごく少量ですができる可能性があります。
2Aペプチドも2Aの下流にある遺伝子の発現量は低下していまいますが、IRESに比べて高いレベルを発現させることができます。こちらの論文 (Sci. Rep. 2017) では、2Aペプチドの前にある遺伝子に比べて、2Aペプチドの後ろにある遺伝子の発現量は2~3割であると報告されています。
2Aペプチドの一部が遺伝子に残ってしまうという弱点はありますが、2Aのサイズは小さいので、2Aペプチドが遺伝子の機能に影響する可能性はそれほど高くはありません。
まとめに代えて
この記事ではIRESと2Aペプチドを紹介しました。
今回は簡単のため2つの遺伝子を発現する方法について述べましたが、もちろんこれらを複数使うことで1つのmRNAから3つ以上の遺伝子を発現させることもできます。
実際、iPS細胞の山中4因子の同定論文でもここで紹介した技術が使われています。
ぜひ研究にお役立てください。
関連図書
この記事に関連した内容を紹介している本はこちらです。
今日も【生命医学をハックする】 (@biomedicalhacks) をお読みいただきありがとうございました。当サイトの記事をもとに加筆した月2回のニュースレターも好評配信中ですので、よろしければこちらも合わせてどうぞ