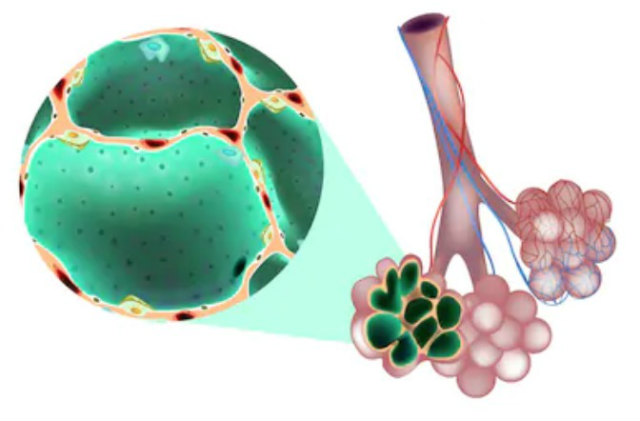
呼吸器感染症と戦うためには、体は免疫の働きを必要としています。免疫に関わるのは主に白血球で、その中にマクロファージと呼ばれる細胞がいます。
マクロファージは通常では病原体を攻撃すると思われてきましたが、肺にはもう1つ、免疫を抑える働きをするマクロファージがいることが分かりました。
この研究成果を、生命科学系の研究者ではない方に向けて噛み砕いて説明します。
免疫が働きすぎると生命に悪影響が及ぶ
血液中を流れる白血球は免疫を担当する細胞です。
この「白血球」というのは好中球やリンパ球など複数の種類の細胞の総称で、その中にはマクロファージと呼ばれる細胞もいます。
マクロファージやその他の免疫系が細胞が協調して病原体と戦いますが、炎症反応が強すぎると生命を脅かす状態へつながることもあります。
マクロファージは病原体を飲み込む (貪食する) ことで殺すというのがよく知られた働きですが、免疫学領域のScience Immunology誌に掲載された論文では、インフルエンザウイルスに感染したマウスの肺では逆の働きをするマクロファージがいることが分かりました。
つまり、肺の過剰な炎症を抑制するマクロファージがいて、生命への悪影響を防いでくれているということです。
もう少し細かく
もう少しだけ詳しく、でも専門用語を使わずに解説します。
この研究は2017年にカマル・カーンナ氏が発表した研究がスタートです。
当時その研究室では、血液濾過器官である脾臓 (ひぞう) にあるマクロファージについて研究していました。染色したマウスの脾臓組織を顕微鏡で見ると、マクロファージは脾臓の免疫細胞が豊富な領域の周りに青いリングを形成して、星雲のような印象的な形態でした。
研究者たちが巧妙な遺伝子戦略でマクロファージを枯渇させたところ、通常ならば排出されるはずのリステリア菌に少量感染したマウスは、わずか2日後に死亡したのです。
また、他の免疫細胞が脾臓にある感染と戦うゾーンに集積していたのに対し、このマクロファージ群はそこには集まっていませんでした。
この観察は、マクロファージが免疫抑制作用を持っていることを示唆していました。通常では根治できずはずのリステリア菌感染で死亡したのは、詳しい解析の結果、過剰な免疫反応が原因だということが分かったからです。
2017年にSience Immunology誌に発表された「CD169+ macrophages orchestrate innate immune responses by regulating bacterial localization in the spleen」は脾臓にいる炎症を抑えるマクロファージについての論文です。
それを受けて、同じ研究グループが行ったのが今回の研究です。
以前から、複雑な肺においては、マクロファージの大部分は肺胞と呼ばれる小さな袋に集まっていることが知られていました。
しかし、研究者たちが顕微鏡下で肺の組織を調べたところ、明らかにこれとは異なる、ずっと小さなマクロファージの集団が見られました。
大きくて丸い、肺胞マクロファージ(alveolar macrophages, AM)とは違って、この新しいタイプのマクロファージは小さく細長い形をしていて、肺胞にはいません。神経・気道関連マクロファージ (NAM, nerve- and airway-associated macrophages) と名付けられたこの新しいマクロファージは、気道に集まり、周囲の神経と相互作用しています。
研究者らは、マウスのAMまたはNAMを枯渇させた後、インフルエンザウイルスに感染させ、インフルエンザウイルス量を比較しました。
これらの実験から従来型のAMはウイルスと戦い、新型のNAMは免疫を抑え組織の損傷を防ぐという、いわば「分業体制」が分かったのです。
新たなマクロファージとコロナウイルス
NAM欠損マウスは、重度の新型コロナウイルス (COVID-19) 患者に見られるいわゆる「サイトカインストーム」(COVID-19: consider cytokine storm syndromes and immunosuppression)に関与するIL-6など、いくつかの炎症性分子を産生します。
Lancet誌に掲載された、中国・武漢でコロナウイルスの治療を受けた191人を対象とした最近の研究 (Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study) では、生存者と比較して、COVID-19で死亡した患者さんでは血中のIL-6レベルが上昇していることが分かっています。
IL-6を抑える薬 (阻害抗体) は関節リウマチの治療に使用されていますが、これをCOVID-19患者の治療に使えないか臨床試験が米国で進んでいます。
つまり、NAMを操作することでCOVID-19によるサイトカインストームや死亡を減らすことができるかもしれません。
この記事で取り上げた研究では、NAMと神経のクロストークが免疫細胞の機能にどのように関係しているかは明らかにされていません。
NAMを枯渇させ、周囲の神経の状態を評価したり、異なるタイプの感染症で気道神経がどのように影響を受けるかを調べることによって、将来の研究でさらに深く解明されていくでしょう。
腸内にいるマクロファージと神経線維の間にあるクロストークが蠕動運動(消化管を動かして食物を移動させること)を制御できることを示唆する研究 (Cell誌 2016)なども考えると、神経と免疫の関連性は興味深いです。
関連図書
この記事に関連した内容を紹介しているサイトや本はこちらです。
今日も【生命医学をハックする】 (@biomedicalhacks) をお読みいただきありがとうございました。









